ΠΑΝΕΛΛΗΝΙΑ ΟΜΑΔΑ ΕΠΑΓΓΕΛΜΑΤΙΩΝ ΥΓΕΙΑΣ
Επικοινωνήστε μαζί μας στο: [email protected]
ΥΠΟΜΝΗΜΑ ΟΜΑΔΑΣ Β
Μεταξύ του Δεκεμβρίου του 2020 και του Μαρτίου του 2021, η Ευρωπαϊκή Επιτροπή Φαρμάκων (E.M.A) έδωσε έγκριση σε 4 εμβόλια ενάντια του SARS – CoV – 2 (severe acute respiratory syndrome coronavirus 2) συμπεριλαμβανομένου και του ChAdOx1 nCov-19 εμβολίου (Astra – Zeneca) [1].
Παρά ταύτα, προς τα τέλη του Φεβρουαρίου του 2021, ένας σημαντικός αριθμός από θρομβώσεις του φλεβικού δικτύου (Venous Thromboses – VTE) σε σπάνια σημεία του φλεβικού δικτύου, όπως οι φλεβώδεις κόλποι του εγκεφάλου (cerebral venous–sinus thrombosis [CVST]) και οι σπλαγχνικές φλέβες (splanchnic vein thrombosis [SVT]), σε συνδυασμό με θρομβοκυτταροπενία, παρατηρήθηκε σε άτομα που έλαβαν το εμβόλιο Astra Zeneca.
Αυτό είχε ως αποτέλεσμα στις 15 Μαρτίου του 2021 η EMA να εισηγηθεί την προσωρινή διακοπή του εμβολίου σε χώρες όπως η Αυστρία, η Γερμανία, Γαλλία, το Ηνωμένο Βασίλειο και η Νορβηγία [2].
Ειδικότερα, στο διάστημα Ιανουαρίου – Απριλίου 2021 (4 μήνες) παρατηρήθηκαν συνολικά 169 κρούσματα CVST και 53 κρούσματα SVT σε 34 εκατομμύρια ανθρώπους που είχαν εμβολιαστεί στην Ευρωπαϊκή Ένωση [2].
Οι Greinacher et al [3], περιέγραψαν κλινικοεργαστηριακά δεδομένα από 11 ασθενείς από Γερμανία και Αυστρία, στους οποίους αναπτύχθηκε Ιδιοπαθής Θρομβωτική Θρομβοπενική Πορφύρα μετά την χορήγηση του ChAdOx1 nCov-19.
Συνολικά 9 στους 11 ασθενείς είχαν CVST, τρεις είχαν SVT και τέσσερις πνευμονική εμβολή.
Από αυτούς τελικά οι έξι κατέληξαν.
Όλοι οι ασθενείς ανέπτυξαν θρομβοπενία, χωρίς κάποιος να έχει λάβει ηπαρίνη πριν από την έναρξη των συμπτωμάτων.
Επιπλέον στην μελέτη προστέθηκαν 28 ασθενείς και άπαντες βγήκαν θετικοί για τα αντισώματα έναντι του παράγοντα 4 των αιμοπεταλίων – ηπαρίνης (PF4).
Οι ερευνητές διαπίστωσαν ότι τα θρομβωτικά θρομβοπενικά σύνδρομα είχαν εντυπωσιακές ομοιότητες με το σύνδρομο θρομβοπενίας προκαλούμενο από ηπαρίνη (HIT), το οποίο ευθύνεται για προθρομβωτικά συμβάντα.
Οι ασθενείς στην μελέτη όμως δεν είχαν λάβει ηπαρίνη !
Η ομάδα του Greinacher πρότεινε να ονοματίσουν αυτό το σύνδρομο που προκαλείται από το εμβόλιο «ανοσοποιητική θρομβωτική θρομβοπενία (Vaccine – induced Thrombocytic Thrombopenia, VITT)».
Οι Schultz et al [4], από το Πανεπιστημιακό Νοσοκομείο του Όσλο, περιέγραψαν πέντε περιπτώσεις εργαζομένων στον τομέα της υγειονομικής περίθαλψης σε σύνολο 130.000 εμβολιασμένων, οι οποίοι εμφάνισαν CVST και Θρομβοπενία, 7-10 ημέρες μετά την λήψη του εμβολίου ChAdOx1 nCov-19. Όλοι οι ασθενείς παρουσίασαν υψηλά επίπεδα αντισωμάτων έναντι του παράγοντα 4 των αιμοπεταλίων και της ηπαρίνης, χωρίς όμως να υπάρχει προηγούμενη έκθεση σε ηπαρίνη.
Η ομάδα των Νορβηγών επιστημόνων κατέληξε στο συμπέρασμα ότι το VITT, παρά το γεγονός ότι το θεωρούσαν ένα σπάνιο αλλά δυνητικά σοβαρό θαμβωτικό επεισόδιο σε νεαρούς ενήλικες, ίσως τελικά να είναι πιο συχνό από το αναμενόμενο [4].
Επίσης έχουν προταθεί και άλλοι μηχανισμοί με τους οποίους τα αιμοπετάλια συσσωματώνονται δημιουργώντας θρόμβους. Ως προς την περίπτωση των εμβολίων που χρησιμοποιούν φορέα – αδενοιό, είναι αποδεδειγμένο ότι αυτοί οι αδενοιοί μπορούν να συνδεθούν με αιμοπετάλια, χρησιμοποιώντας τον υποδοχέα coxsackie – adenovirus (CAR) ο οποίος αποτελεί ένα αρχικό βήμα εισόδου του ιού στα αιμοπετάλια [5].
Τα εμβόλια ChAdOx1 nCov-19 είναι αποδεδειγμένο ότι χρησιμοποιούν τον CAR υποδοχέα [6].
Τα εμβόλια Ad26.COV2.S (Johnson & Johnson / Janssen), χρησιμοποιούν μια ανασυνδυασμένη έκδοση (με ανεπάρκεια αντιγραφής) του ανθρώπινου αδενοιού που δεν φέρει τον υποδοχέα CAR, πλην όμως, σε αυτά τα εμβόλια το σιαλικό οξύ στα αιμοπετάλια είναι ο υποδοχέας πρόσδεσης.
Τα ανθρώπινα αιμοπετάλια είναι γνωστό ότι διαφέρουν ως προς την περιεκτικότητα σε σιαλικό οξύ, το οποίο έχει εμπλακεί στη συσσωμάτωση και προσκόλλησή τους και μπορεί να παίζει ρόλο σε διαταραχές των αιμοπεταλίων όπως η θρομβοκυτταροπενία [7].
Επομένως, οι αλληλεπιδράσεις των φορέων ChAdOx1 και Ad26.COV2.S με αιμοπετάλια είναι εύλογες, ειδικά δεδομένου ότι κάθε ενδομυϊκά ενέσιμη δόση αυτού του εμβολίου περιέχει 5 × 1010 ιικά σωματίδια [8].
Επιπλέον, όπως αποδεικνύεται με χρήση ανθρώπινου αδενοϊού τύπου 5, και ανθρώπινου αδενοϊού τύπου 3, η δέσμευση αδενοϊικών σωματιδίων σε κυκλοφορούντα αιμοπετάλια μπορεί να ενεργοποιήσει τα τελευταία και να οδηγήσει στη συσσωμάτωσή τους [8].
Είναι επίσης σημαντικό να γνωρίζουμε εάν το σύμπλοκο αδενοϊού-αιμοπεταλίων μπορεί να προκαλέσει από μόνο του την αυτοάνοση απόκριση, ιδιαίτερα παρουσία των προϋπάρχοντων αντισωμάτων κατά του PF4.
Συγκεκριμένα, προηγούμενες μελέτες σε τρωκτικά, κουνέλια και πρωτεύοντα, πλην του ανθρώπου, έδειξαν ότι η ενδοφλέβια χορήγηση αδενοϊικών φορέων μπορεί να οδηγήσει σε οξεία θρομβοκυτταροπενία και πήξη με έναρξη εντός 24 ωρών [8].
Τα δυο εμβόλια AZD1222 και Ad26.COV2.S χορηγούνται ενδομυϊκά, και σύμφωνα με τη μελέτη βιοκατανομής σε ποντίκια BALB / c, ο υψηλότερος αριθμός ιογενών αντιγράφων παρατηρείται στον σκελετικό μυ στη θέση χορήγησης, με χαμηλά επίπεδα σποραδικά σε άλλους ιστούς – καρδιά, ήπαρ, λεμφαδένες, ωοθήκες και όρχεις (μελέτη 0841MV38.001) [8].
Επιπλέον πιθανολογείται ότι υπάρχει διασταυρούμενη αντιδραστικότητα των αντισωμάτων έναντι της πρωτεϊνικής ακίδας με τον παράγοντα 4 των αιμοπεταλίων (PF4). Η διασταυρούμενη αντιδραστικότητα εμφανίζεται, όταν ένα αντίσωμα που στρέφεται εναντίον ενός συγκεκριμένου αντιγόνου, αναγνωρίζει επιτυχώς επιτόπους άλλων αντιγόνων. Υπάρχει πιθανή διασταυρούμενη αντιδραστικότητα μεταξύ των αντισωμάτων έναντι της πρωτεϊνικής ακίδας και διαφορετικών πρωτεϊνών, όπως είναι η βασική πρωτεΐνη μυελίνης, οι τρανσγλουταμινάσες 2 και 3, τα μιτοχόνδρια, το πυρηνικό αντιγόνο, η α- μυοσίνη, η υπεροξειδάση του θυρεοειδούς και το κολλαγόνο [8].
Ένας ακόμα πιθανός μηχανισμός, ο οποίος βρίσκεται υπό μελέτες, είναι οι διασταυρούμενη αντιδραστικότητα των αντισωμάτων του ανθρώπινου ανασυνδυασμένου αδενοϊού, με τον παράγοντα 4 των αιμοπεταλίων [8].
Υπάρχει ξεκάθαρη αλληλεπίδραση μεταξύ της πρωτεϊνικής ακίδας και του υποδοχέα του μετατρεπτικού ένζυμου της αγγειοτενσίνης -2 (ACE2) στην επιφάνεια των αιμοπεταλίων, τόση που είναι επαρκής για να ενισχύσει την προθρομβωτική λειτουργία !
Επομένως, αυτό το εύρημα οδηγεί στο κρίσιμο ερώτημα, κατά πόσο η πρωτεϊνική ακίδα που παράγεται μετά από εμβολιασμό με εμβόλια φορέα ή mRNA μπορεί (και πόσο συχνά) να εκκρίνεται σε ελεύθερη μορφή, να εμφανίζεται στο αίμα και πιθανώς να αλληλεπιδράσει με αιμοπετάλια με παρόμοιο τρόπο.
Μετά τον εμβολιασμό (φορέα και mRNA) και την παραγωγή των ακίδων πρωτεΐνης, αυτές με την σειρά τους αποικοδομούνται περαιτέρω σε αντιγονικά πεπτίδια και παρουσιάζονται σε κυτταροτοξικά Τ λεμφοκύτταρα μέσω του κύριου μονοπατιού ιστοσυμβατότητας (MHC) Ι, αλλά μπορούν επίσης να απελευθερωθούν και να ληφθούν από δενδριτικά κύτταρα και να παρουσιαστούν περαιτέρω σε βοηθητικά Τ κύτταρα και Β κύτταρα μέσω του μονοπατιού MHC II !!
Δεν μπορεί, επομένως, να αποκλειστεί ότι μπορεί να συμβεί σποραδική διαφυγή των πρωτεϊνικών ακίδων κατά την μεταφορά τους [8] !!
Στις 9 Ιουνίου 2021, η ιατρός Tess Lawrie, από το Ηνωμένο Βασίλειο, εξέδωσε δημόσια τα αποτελέσματα των κίτρινων καρτών για τα εμβόλια COVID-19 την περίοδο μεταξύ 8.12.2020 και 6.5.2021:
Κατά την διάρκεια αυτής της πεντάμηνης περιόδου 24 εκατομμύρια άτομα έλαβαν και τις δυο δόσεις στο Ηνωμένο Βασίλειο. Η ιατρός Lawrie κρούει τον κώδωνα του κινδύνου, δεδομένου ότι σε αυτό το διάστημα των πέντε μηνών σημειώθηκαν 1253 θάνατοι και 888.196 ανεπιθύμητες αντιδράσεις που σχετίστηκαν με τα εμβόλια COVID-19 !!!
Η ιατρός χωρίζει τις ανεπιθύμητες ενέργειες σε 6 κλινικές κατηγορίες [9].
-Στην 1η κλινική κατηγορία ανήκουν οι αιμορραγίες, οι θρομβώσεις και τα ισχαιμικά επεισόδια.
Η συγκεκριμένη κατηγορία ονομάστηκε, επίσης, και ως η ομάδα του θανάτου (!), εκ του δραματικού γεγονότος ότι υπήρξαν πολλοί ξαφνικοί θάνατοι: 438 !!
Θεώρησαν ότι το πιθανό αίτιο (σύμφωνα με τα κλινικά ευρήματα και τις εξετάσεις που έγιναν), θα μπορούσε να είναι τα αιμορραγικά, θρομβοεμβολικά – ισχαιμικά επεισόδια στον εγκέφαλο. Είχαν προκύψει ήδη κυβερνητικές εκθέσεις, σχετικά με την εμφάνιση εγκεφαλικών επεισοδίων σε έδαφος θρόμβωσης των φλεβωδών κόλπων του εγκεφάλου (24 θάνατοι, 226 ανεπιθύμητα επεισόδια). Ωστόσο, η ανάλυση δεδομένων που έγινε κατέληξε στο συμπέρασμα ότι οι θρομβοεμβολικές ανεπιθύμητες ενέργειες θα μπορούσαν να αφορούν σχεδόν όλες τις φλέβες και τις αρτηρίες, συμπεριλαμβανομένων μεγάλων αγγείων, όπως η αορτή, τα αγγεία στον εγκέφαλο, την καρδιά, τον σπλήνα, τα νεφρά, τις ωοθήκες, το ήπαρ, και θα μπορούσαν να είναι απειλητικές για την ζωή ή να καταστρέψουν την ποιότητα ζωής του εμβολιασμένου [9] !!!
-Στην 2η κλινική κατηγορία υπάρχουν οι ανεπιθύμητες αντιδράσεις που σχετίζονται με το ανοσοποιητικό σύστημα.
Υπήρξαν επανενεργοποιήσεις λανθανόντων ιών, όπως του έρπητα ζωστήρα και της λύσσας !!
Αυτό υποδηλώνει ανοσοανεπάρκεια που προκαλείται από τα εμβόλια !!
Επίσης προέκυψε διαταραχή του ανοσοποιητικού συστήματος που συσχετιζόταν με τα εμβόλια, με αποτέλεσμα να εμφανιστούν αυτοάνοσες παθήσεις όπως το σύνδρομο Guillain-Barré (280 περιπτώσεις, 6 θάνατοι), Κολίτιδες Crohn και Ελκώδης (231 περιπτώσεις, 2 θάνατοι) και σκλήρυνση κατά πλάκας (113 περιπτώσεις) !!
Επιπλέον, υπήρξαν πολλές αλλεργικές αντιδράσεις (25,.70) εκ των οποίων 4 ήταν θανατηφόρες και 1.001 εμβολιασμένοι υπέστησαν οξύ αναφυλακτικό σοκ [9] !!
-Στην 3η κλινική κατηγορία υπάρχουν ανεπιθύμητες αντιδράσεις που σχετίζονται με το άλγος, όπως αρθραλγίες (24.902 περιπτώσεις), μυαλγίες (31.168 περιπτώσεις), ινομυαλγίες (270 περιπτώσεις) και κεφαλαλγίες (90.000 περιπτώσεις) [9].
-Στην 4η κλινική κατηγορία υπάρχουν νευρολογικές ανεπιθύμητες αντιδράσεις. Εδώ ανήκει το 21% των συνολικών ανεπιθύμητων αντιδράσεων (185.474 περιπτώσεις). Παρατηρήθηκε μεγάλη ποικιλία νευρολογικών αντιδράσεων, από τις πιο συχνές που ήταν επιληπτικές κρίσεις (1,992 περιπτώσεις), κάποιας μορφής παραλύσεις (2,357 περιπτώσεις), παράλυση του Bell (626 περιπτώσεις), έως τις πιο σπάνιες όπως εγκεφαλοπάθεια, άνοια, αταξία και παρκινσονισμούς [9] !!
-Στην 5η κλινική κατηγορία υπήρξαν ανεπιθύμητες αντιδράσεις που σχετίζονται με απώλεια όρασης, ακοής και όσφρησης καθώς και διαταραχής του λόγου [9].
-Στην 6η κλινική κατηγορία υπάρχουν ανεπιθύμητες αντιδράσεις στην εγκυμοσύνη. Οι έγκυοι αποτελούσαν ένα μικρό ποσοστό των εμβολιασμένων στο Ηνωμένο Βασίλειο. Παρ’ όλα αυτά, φαίνεται να υπάρχει μεγάλος αριθμός ανεπιθύμητων αντιδράσεων (307), συμπεριλαμβανομένου ενός θανάτου εγκύου, ένα θάνατος νεογνού μετά από πρόωρο τοκετό και 150 αυθόρμητες αμβλώσεις [9].
Η άποψη της ιατρού είναι ότι οι ανεπιθύμητες ενέργειες δεν περιορίζονται σε κάποια συγκεκριμένο εμβόλιο COVID-19 [9].
*Στην άδεια κυκλοφορίας του EMA του εμβολίου Pfizer Biontech, στη σελίδα 4 αναφέρεται ότι το εμβόλιο εξαιρείται μελετών για αλληλεπίδραση με άλλα φάρμακα.
Στην ίδια σελίδα αναφέρει ότι υπάρχουν περιορισμένα δεδομένα για χρήση του σε εγκύους, καθώς και ότι μελέτες έχουν γίνει αφορούν μόνο τα ζώα.
Επιπλέον, αναφέρεται ότι η διάρκεια προστασίας που παρέχει το εμβόλιο είναι άγνωστη, καθώς το σκεύασμα βρίσκεται ακόμα υπό κλινικές μελέτες !!
Χαρακτηριστικό είναι δε, ότι στη σελίδα 11 αναφέρεται ρητά ότι το συγκεκριμένο εμβόλιο εξαιρείται από μελέτες γονοτοξικότητας και καρκινογένεσης !!!
ΓΙΑΤΙ;
Τέλος, στη σελίδα 21 αναφέρεται ότι η ημερομηνία λήξης των κλινικών μελετών για το εμβόλιο Pfizer Biontech είναι ο 12ος/2023. Η μελέτη που πραγματοποιείται είναι τυφλή τυχαιοποιημένη ελεγχόμενη με εικονικό φάρμακο (placebo) [10].
*Παρόμοια εικόνα παρατηρείται για το εμβόλιο της Moderna. Στη σελίδα 4 της άδειας ΕΜΑ κυκλοφορίας του εμβολίου, αναφέρεται επίσης ότι και το εμβόλιο αυτό εξαιρείται μελετών για αλληλεπίδραση με άλλα φάρμακα. Επιπλέον, αναφέρεται ότι η διάρκεια προστασίας που παρέχει το εμβόλιο είναι άγνωστη (!!(, καθώς το σκεύασμα βρίσκεται ακόμα υπό κλινικές μελέτες.
Στην παράγραφο 5.3, στη σελίδα 9 αναφέρεται ότι και το εμβόλιο Moderna απαλλάσσεται από μελέτες γονοτοξικότητας και καρκινογένεσης.
ΓΙΑΤΙ;
Τέλος στη σελίδα 15, ενότητα Ε, αναφέρει ότι οι μελέτες του συγκεκριμένου εμβολίου θα λήξουν τον 12ο/2022.
Όπως και με το εμβόλιο της Pfizer Biontech, η μελέτη που πραγματοποιείται είναι τυφλή τυχαιοποιημένη ελεγχόμενη με εικονικό φάρμακο (placebo) [10].
*Στην άδεια κυκλοφορίας του ΕΜΑ του εμβολίου Astra Zeneca, στη σελίδα 5, υποενότητα 4.5, αναφέρεται επίσης ρητά ότι και το εμβόλιο αυτό εξαιρείται μελέτης αλληλεπίδρασης με άλλα φάρμακα.
Στη σελίδα 4 αναφέρεται ότι η διάρκεια προστασίας που παρέχει το εμβόλιο είναι και εδώ άγνωστη, καθώς και εδώ το σκεύασμα βρίσκεται υπό κλινικές δοκιμές.
Στη σελίδα 10, υποενότητα 5.3, αναφέρεται και εδώ ρητά ότι για το συγκεκριμένο εμβόλιο δεν έγιναν μελέτες καρκινογένεσης και γονοτοξικότητας.
ΓΙΑΤΙ;
Τέλος, στη σελίδα 17, αναφέρεται ότι καταληκτική ημερομηνία για τις κλινικές μελέτες του εμβολίου της Astra Zeneca είναι η 31η Μαρτίου του 2024, με τις μελέτες να είναι τυχαιοποιημένες – ελεγχόμενες [10].
*Τέλος, για το εμβόλιο Johnson & Johnson, στην άδεια κυκλοφορίας του ΕΜΑ, στη σελίδα 4 αναφέρεται ότι οι επιστήμονες υγείας πρέπει να έχουν αυξημένη εγρήγορση για συμπτώματα και σημεία θρομβοεμβολής ή/ και θρομβοπενίας !!
Στην ίδια σελίδα, παρομοίως με τα προηγούμενα εμβόλια, αναφέρεται ότι η διάρκεια προστασίας που παρέχει το εμβόλιο είναι άγνωστη, καθώς το σκεύασμα βρίσκεται υπό κλινικές δοκιμές.
Όπου κλινική, και για τα τέσσερα εμβόλια, η ανθρωπότητα…
Στη σελίδα 5, αναφέρει ότι εξαιρείται από μελέτες αλληλεπίδρασης με άλλα φάρμακα.
Στη σελίδα 11, υποενότητα 5.3, αναφέρεται ότι και το εμβόλιο Jansen δεν έχει αξιολογηθεί ως προς την ενδεχόμενη καρκινογονική και γονοτοξική δράση του.
ΓΙΑΤΙ;
Και όλα τα υπόλοιπα «γιατί»…
Τέλος, στη σελίδα 20, ενότητα Ε, αναφέρεται ότι οι μελέτες είναι τυφλές – τυχαιοποιημένες, ελεγχόμενες με εικονικό φάρμακο (placebo) και ολοκληρώνονται την 31η Δεκεμβρίου του 2023 [10].
Εκπληκτικό είναι επίσης το γεγονός, ότι ο FDA, σχετικά με το εμβόλιο της Pfizer Biontech, αναφέρει ότι η επιστημονική κοινότητα δεν έχει ενδείξεις σχετικά με το κατά πόσο το εμβόλιο σταματάει ή μειώνει την μετάδοση του ιού από άνθρωπο σε άνθρωπο [11] !!!
Νέα μελέτη, των καθηγητών Harald Walach, Rainer Klement και του Ολλανδού αναλυτή δεδομένων Wouter Aukema, δημοσιεύθηκε (πλήρως αξιολογημένη) στο MDPI στις 24 Ιουνίου 2021. Τα πραγματικά δεδομένα σχετικά με τον αριθμό των εμβολιασμών που απαιτούνται για την πρόληψη ενός θανάτου προέρχονται από μια μεγάλη ισραηλινή μελέτη πεδίου. Από αυτό το πεδίο, υπολογίστηκε ο αριθμός των εμβολιασμών (NNTV – Numbers Needed To Vaccinate) που απαιτούνται για την πρόληψη ενός θανάτου. Οι ανεπιθύμητες αντιδράσεις φαρμάκων (ADR) ελήφθησαν από τη βάση δεδομένων του Ευρωπαϊκού Οργανισμού Φαρμάκων και το ολλανδικό εθνικό μητρώο (lareb.nl) από τις 28 Μαΐου 2021, για να εξαχθεί ο αριθμός των περιπτώσεων με σοβαρές ανεπιθύμητες παρενέργειες και ο αριθμός των θανατηφόρων περιπτώσεων.
Το τρομακτικό αποτέλεσμα της μελέτης:
Για τρεις θανάτους που αποτρέπονται από τον εμβολιασμό, πρέπει να δεχτούμε δύο θανάτους που προκαλούνται από τον εμβολιασμό !!!
Οι συγγραφείς καταλήγουν στο πολύ σοβαρό συμπέρασμα, ότι η προφανής έλλειψη σαφούς οφέλους θα πρέπει να ωθήσει τις κυβερνήσεις να επανεξετάσουν τις πολιτικές εμβολιασμού !!
Χαρακτηριστική δε είναι η αναφερόμενη ελλιπής παρουσία δεδομένων. Ο ευρωπαϊκός μέσος όρος είναι 127 ατομικές αναφορές ασφάλειας (ICSR), δηλαδή περιπτώσεις με αναφορές ανεπιθύμητων παρενεργειών ανά 100.000 εμβολιασμούς.
Ωστόσο:
Οι ολλανδικές αρχές έχουν καταγράψει 701 αναφορές ανά 100.000 εμβολιασμούς, ενώ η Πολωνία έχει μόνο 15 ISCR ανά 100.000 εμβολιασμούς.
Υποθέτοντας ότι η διαφορά αυτή δεν οφείλεται σε διαφορετική εθνική ευαισθησία στα ανεπιθύμητα συμβάντα των εμβολίων, αλλά σε διαφορετικά εθνικά πρότυπα αναφοράς, οι συγγραφείς αποφάσισαν να χρησιμοποιήσουν δεδομένα από το ολλανδικό εθνικό μητρώο (https://www.lareb.nl/coronameldingen, πρόσβαση στις 29 Μαΐου 2021), για να μετρήσουν τον αριθμό των σοβαρών και θανατηφόρων ανεπιθύμητων συμβάντων ανά 100.000 εμβολιασμούς. Τα δεδομένα αυτά συγκρίθηκαν με το NNTV, για την πρόληψη ενός κλινικού περιστατικού και ενός θανάτου από την COVID-19 [12].
Στην τεχνική ενημερωτική έκθεση Νο17 που εκπόνησε ο Οργανισμός Δημόσιας Υγείας του Ηνωμένου Βασιλείου, με τίτλο «SARS – CoV -2 variants of concern and variants under investigation in England», και η οποία δημοσιεύτηκε στις 25 Ιουνίου [13], γίνεται αναλυτική ενημέρωση για τις διάφορες μεταλλάξεις του SARS – CoV – 2, τα οποία προκάλεσαν μεγάλη αίσθηση στο Ηνωμένο Βασίλειο.
Στον πίνακα 4 της εν λόγω έκθεσης, δίνονται στατιστικά στοιχεία για τα κρούσματα της μετάλλαξης Δέλτα (variant Delta), τις νοσηλείες και τους θανάτους από το εν λόγω στέλεχος του ιού.
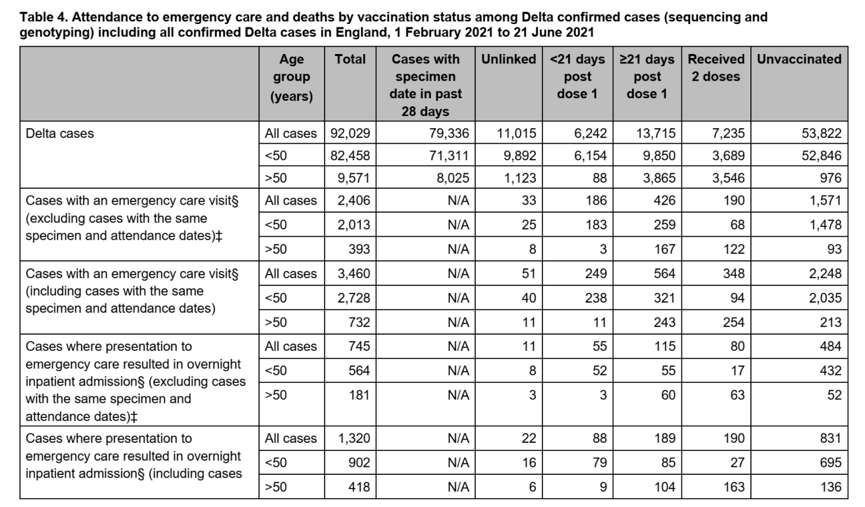
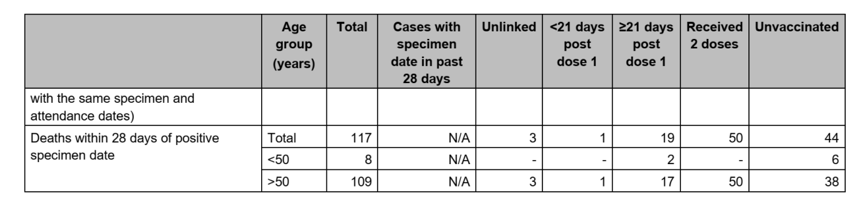
Από τα στοιχεία του πίνακα 4 προκύπτουν τα εξής:
Περιστατικά μεταξύ μη εμβολιασμένων: 53.822
Θάνατοι μεταξύ μη εμβολιασμένων: 44
Αδρός Δείκτης Θνητότητας στους μη εμβολιασμένους: 44/53.822 = 0,082%
Περιστατικά μεταξύ εμβολιασμένων: 27.192
Θάνατοι μεταξύ εμβολιασμένων: 70
Αδρός Δείκτης Θνητότητας στους εμβολιασμένους: 70/27.192 = 0,26%
Με βάση τα δεδομένα από την Αγγλία, η μετάλλαξη Δέλτα, αν και έπιασε περισσότερο τους μη εμβολιασμένους (53.822 έναντι 27.192 περιστατικών), υπήρξε πολύ περισσότερο θανατηφόρος στους εμβολιασμένους από όσο στους μη εμβολιασμένους:
Σχεδόν τριπλάσια θνητότητα [13] !!!
Αν και από τα εν λόγω δεδομένα δεν μπορούμε να αποφανθούμε για το πού ακριβώς οφείλεται η παρατηρούμενη διαφορά στη θνητότητα μεταξύ εμβολιασμένων και μη, εντούτοις, καθίσταται απολύτως ξεκάθαρο ότι ο ιός εξακολουθεί να μεταδίδεται και μεταξύ των εμβολιασμένων:
Και μάλιστα να τους πλήττει περισσότερο !!!
Ώστε, ο όποιος διαχωρισμός των ανθρώπων σε εμβολιασμένους και ανεμβολίαστους είναι επιστημονικά, και μετά ταύτα και νομικά, απαράδεκτος !!!
ΟΜΑΔΑ Β:
ΒΙΒΛΙΟΓΡΑΦΙΑ:
1).European Centre for Disease Prevention and Control COVID-19 Vaccine Tracker. https://qaq.ecdc.europa.eu/public/extensions/COVID19/vaccine-tracker.html.
2). Mateo Porres-Aguilar, Alejandro Lazo-Langner, Arturo Panduro, and Misael Uribe. COVID-19 vaccine-induced immune thrombotic thrombocytopenia: An emerging cause of splanchnic vein thrombosis. Ann Hepatol. 2021 July-August; 23: 100356.
3). Greinacher A., Thiele T., Warkentin T.E., Weisser K., Kyrle P.A., Eichinger S. Thrombotic thrombocytopenia after ChAdOx1 nCov-19 vaccination. N Engl J Med. 2021;(April) doi: 10.1056/NEJMoa2104840.
4). Schultz N.H., Sørvoll I.H., Michelsen A.E., Munthe L.A., Lund-Johansen F., Ahlen M.T. Thrombosis and thrombocytopenia after ChAdOx1 nCoV-19 vaccination. N Engl J Med. 2021;(April) doi: 10.1056/NEJMoa2104882.
5). Gupalo E., Buriachkovskaia L., Othman M. Human platelets express CAR with localization at the sites of intercellular interaction. Virol. J. 2011;8:456. doi: 10.1186/1743-422X-8-456.
6). Dicks M.D.J., Spencer A.J., Coughlan L., Bauza K., Gilbert S.C., Hill A.V.S., Cottingham M.G. Differential immunogenicity between HAdV-5 and chimpanzee adenovirus vector ChAdOx1 is independent of fiber and penton RGD loop sequences in mice. Sci. Rep. 2015;5:16756. doi: 10.1038/srep16756.
7). Baker A.T., Mundy R.M., Davies J.A., Rizkallah P.J., Parker A.L. Human adenovirus type 26 uses sialic acid–bearing glycans as a primary cell entry receptor. Sci. Adv. 2019;5:eaax3567. doi: 10.1126/sciadv.aax3567.
8). Piotr Rzymski, Bartłomiej Perek, and Robert Flisiak. Thrombotic Thrombocytopenia after COVID-19 Vaccination: In Search of the Underlying Mechanism. Vaccines (Basel). 2021 Jun; 9(6): 559.
9). Dr. Tess Lawrie. RE: Urgent preliminary report of Yellow Card data up to 26th May 2021. Medicines and Healthcare Products Regulatory Agency.
10).https://www.ema.europa.eu/en/documents/product-information/comirnaty-epar-product-information_el.pdf. https://www.ema.europa.eu/en/documents/product-information/covid-19-vaccine-janssen-epar-product-information_el.pdf. https://www.ema.europa.eu/en/documents/product-information/vaxzevria-previously-covid-19-vaccine-astrazeneca-epar-product-information_el.pdf
12). https://www.eyewideopen.org/?p=1490, Harald Walach1,2,3,*, Rainer J. Klement4and Wouter Aukema. The Safety of COVID-19 Vaccinations—We Should Rethinkthe Policy. Vaccines2021,9, 693. https://doi.org/10.3390/vaccines9070693.
13). Public Health England. SARS-CoV-2 variants of concern and variants under investigation in England Technical briefing 17 25 June 2021
και συνεχίζουμε:
Κάποιες επιπλέον επιστημονικές επισημάνσεις
Παθοφυσιολογικοί μηχανισμοί βλάβης και ανεπιθύμητες ενέργειες
Συσχέτιση ψυχικών ασθενειών με τη νόσο και τα εμβόλια έναντι του sars-cov-2
ΠΑΝΕΛΛΗΝΙΑ ΟΜΑΔΑ ΕΠΑΓΓΕΛΜΑΤΙΩΝ ΥΓΕΙΑΣ
Επικοινωνήστε μαζί μας στο: [email protected]